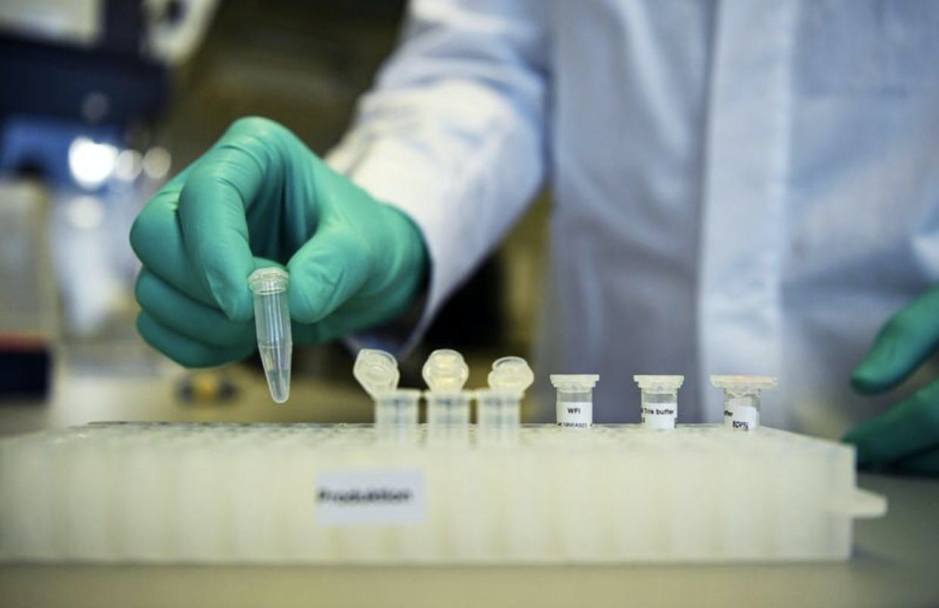
La compañía alemana explicó que la vacuna CVnCoV está basada en la tecnología de ácido ribonucleico mensajero (ARNm), la cual le proporciona al cuerpo la información necesaria para que pueda generar sus propias defensas contra esta enfermedad.
La biofarmacéutica alemana CureVac informó que ha iniciado la segunda fase de investigación clínica de su candidata a vacuna contra la COVID-19, cuyos estudios de confirmación de dosis (CV-NCOV-002) se están llevando a cabo en Perú y Panamá. Participarán un total de 690 personas sanas en dos grupos distintos: adultos mayores de 61 años y participantes más jóvenes entre 18 y 60 años.
«Este estudio también permitirá ampliar la base de datos de seguridad de la vacuna para preparar el inicio de las siguientes fases del estudio 2b y 3. Se espera tener los primeros datos completos de la fase 2a en adultos mayores durante el cuarto trimestre de 2020», dijo la empresa en un comunicado.
Además, precisó que las vacunas se aplicarán en zonas con alta incidencia de infecciones de COVID-19, y se evaluará la respuesta inmune humoral (generación de defensas contra el virus, como los anticuerpos), después de haberla administrado.
Un paso importante
El diseño del estudio fue aprobado y coordinado por las autoridades sanitarias y los comités de ética de Perú y Panamá.
«Está pendiente recibir datos adicionales del estudio de fase 1 y fase 2a. CureVac planea iniciar el ensayo de investigación clínica global de Fase 2b/3 en el que participarán aproximadamente 30 000 personas durante el último trimestre de 2020», refirió la compañía.
Se basa en los datos preliminares de seguridad e inmunogenicidad del estudio de CureVac de Fase 1 CV-NCOV-001 que se está llevando a cabo en adultos sanos voluntarios en Alemania y Bélgica.
«El inicio de la fase 2a del ensayo clínico en Perú y Panamá representa un paso importante hacia adelante en nuestro programa del ensayo clínico de COVID-19», dijo Mariola Fotin-Mleczek, directora de Tecnología de CureVac.
«Este ensayo está diseñado para reforzar la confirmación de la dosis seleccionada de nuestra vacuna candidata y confirmar que podemos proporcionar una vacuna segura y tolerable a los adultos mayores, quienes tienen el mayor riesgo de sufrir un impacto grave de COVID-19», agregó Fotin-Mleczek.