Ante el panorama complicado e incierto producto de la pandemia que esta viviendo el mundo gracias al coronavirus (COVID-19), existe un camino que puede ser beneficioso para los gobiernos que tienen la tarea de emplear planes para combatir esta enfermedad.
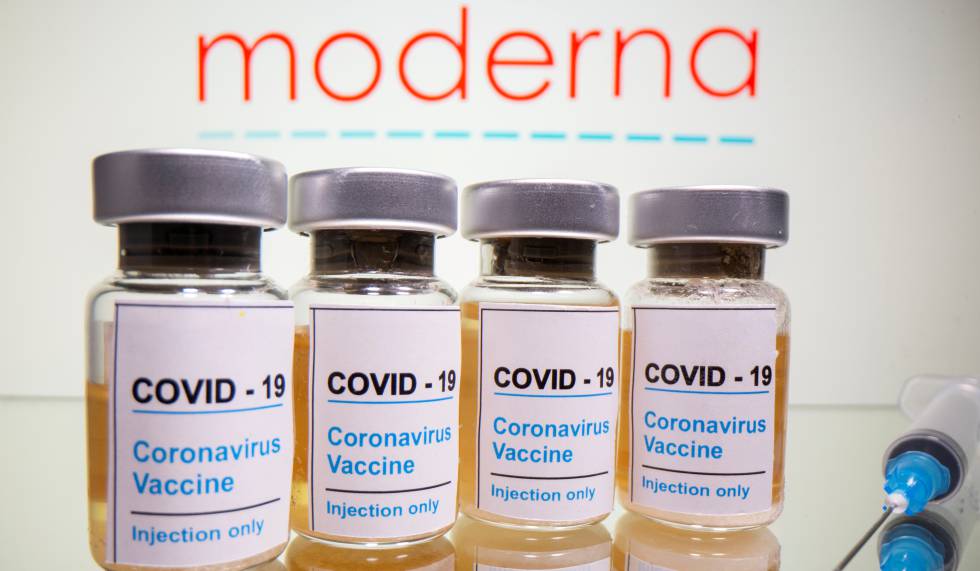
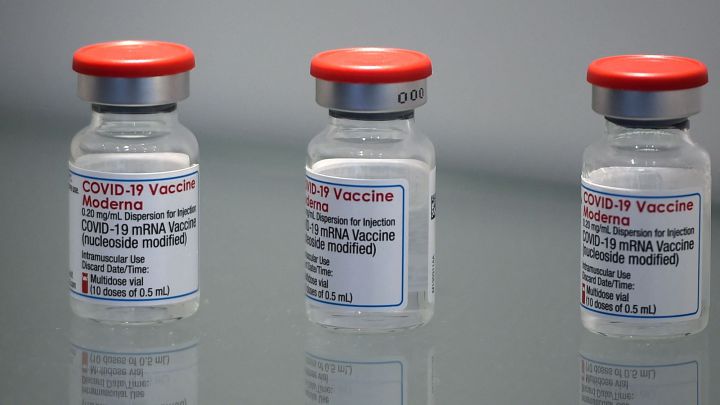
Recientemente, el programa COVAX (conocido como el Fondo de Acceso Global para las Vacunas COVID-19) mantiene un convenio con Moderna (vacuna peruana) para adquirir 500 millones de vacunas, anunció hoy la Alianza de la Vacuna (Gavi).
«Estamos muy contentos de firmar este nuevo acuerdo con Moderna, que da a los participantes de Covax acceso a otra vacuna altamente eficaz», comentó Seth Berkley, director ejecutivo de Gavi en un comunicado oficial. El plan de este importante pacto es que la primera dosis de vacunas deberán ser entregadas en el cuarto trimestre del 2021, «con un total de 34 millones disponibles este año” y «hasta 466 millones de dosis en 2022”.
Es importante señalar que, Moderna se administra mediante dos dosis respectivas, aunque en las recomendaciones indican una sola si es que anteriormente el paciente haya contenido el virus. Además, hay opciones que permiten que la población reciba eventualmente una dosis acomodada a variantes como ‘la brasileña’ y ‘sudafricana’, señaló la organización cuya sede se encuentra en Ginebra.
El origen de este importante unión proviene desde que la Organización Mundial de la Salud (OMS) quienes otorgaron el pasado viernes su homologación de emergencia a la vacuna contra el COVID-19 de Moderna, la quinta en recibir esta aprobación de la agencia sanitaria de la ONU. Por el momento la OMS ha aprobado el uso de la vacuna Pfizer-BioNTech, los dos sueros de AstraZeneca fabricados en India, en Corea del Sur y el de Johnson & Johnson, llamado Janssen.
¿Qué es la vacuna Moderna?
Es una vacuna que fue creada por el Instituto Nacional de Alergias y Enfermedades Infecciosas, la Autoridad del Desarrollo Biomédico Avanzado (BARDA) y por la empresa que tiene el mismo nombre. El análisis de su eficazia se basó en ensayos clínicos doble ciego. Todos los participantes (28.000) partían con un estado inicial negativo de SARS-CoV-2. Recibieron 2 dosis del producto en investigación por programa sin desviaciones importantes del protocolo. El criterio de valoración principal fue la eficacia de la vacuna (EV) para prevenir que el COVID-19 definido por el protocolo, se produzca al menos 14 días después de la segunda dosis. Su comprobación se centra en los datos del primer momento del análisis intermedio preespecificado que consta de 95 casos adjudicados.